您好,欢迎访问天津市纽森科技有限公司官网
全国咨询热线:
022-59590868转812

氮气电化反应合成氨气介绍
技术中心
/ 2024-07-19 00:00:00
背景
电化学合成氨气的原理
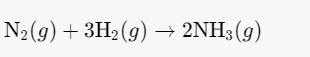
在电化学系统中,这一反应可以分解为两个半反应:
1. 阴极反应(还原反应):
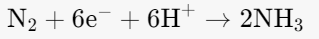
2. 阳极反应(氧化反应):

催化剂
电化学合成氨气的关键在于高效催化剂的开发,常见的催化剂包括:
- 金属催化剂:如钌(Ru)、铂(Pt)、钼(Mo)等。
- 非金属催化剂:如氮化物、碳基材料等。
- 合金催化剂:通过合金化改进催化剂性能。
优势和挑战
优势
1. 节能环保:电化学方法在常温常压下进行,能耗低且减少了对环境的影响。
2. 可再生能源利用:可以结合可再生能源(如太阳能、风能)提供电能,实现绿色氨气合成。
3. 分散生产:电化学合成装置可以较小规模分布使用,适合分散生产。
挑战
1. 催化剂开发:高效、稳定的催化剂材料开发仍是难点。
2. 电能效率:如何提高电能转化效率,降低成本。
3. 工艺优化:反应条件、设备设计等方面的优化需要进一步研究。
结论
最新动态
- 探秘工业制造:从浇铸到3D打印的十四种神奇工艺 2024-08-30 00:00:00
- 氮气在离子膜生产中的关键作用 2024-08-29 00:00:00
- 聚丙烯酰胺(PAM)、聚合硫酸铁(PFS)、聚合氯化铝(PAC)和硫酸亚铁的生产中为什么要使用氮气? 2024-08-27 00:00:00
- 提升水处理效率与安全性:氮气在气浮法中的创新应用 2024-08-26 00:00:00
- 深入解析制氮机空氮比:提升工业气体利用效率的关键 2024-08-20 00:00:00
- 专业的PSA变压吸附制氮机生产厂家-纽森制氮 2024-08-09 00:00:00
- 阀门如何选择、安装、保养、操作和检修。 2024-08-08 00:00:00
- 阀门的功能、分类和基本参数 2024-08-07 00:00:00
- 移动式车载制氮机的相关介绍 2024-08-06 00:00:00
- 用户购买制氮机前需要了解的四大成本因素,你了解多少? 2024-08-05 00:00:00


微信公众号
售后部:022-59590865转822
技术部:022-59590868转821
邮箱:nc@tjnc.cn
公司地址:天津市静海县经济开发区中央大道9号

微信公众号
扫一扫关注我们
微信小程序
扫一扫关注我们
全国销售热线:
022-59590865转812
